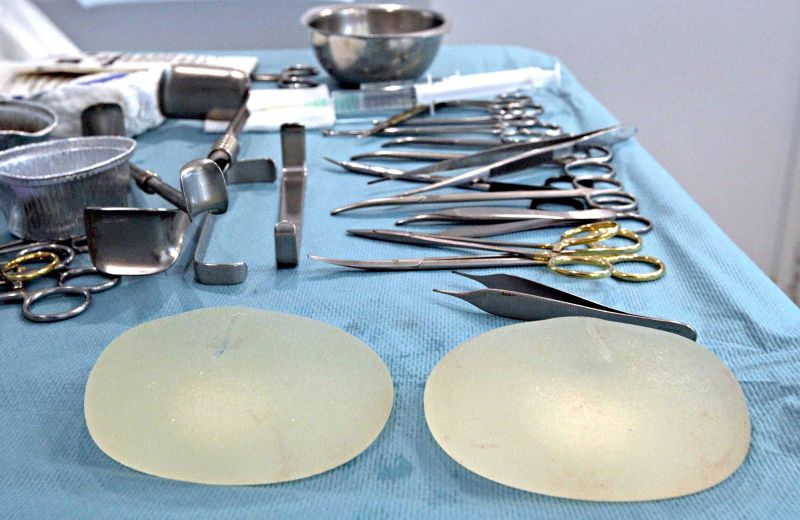
A partir de hoje, a comercialização de novos modelos de próteses mamárias de silicone nacionais e importadas está suspensa temporariamente no país. Uma resolução da Agência Nacional de Vigilância Sanitária (Anvisa) obriga todos os produtos ainda não cadastrados a passarem pela certificação do Instituto Nacional de Metrologia, Qualidade e Tecnologia (Inmetro) antes da entrada no mercado.
Até ontem, importadoras e fabricantes nacionais precisavam apenas apresentar documentos que atestassem a qualidade dos implantes para obter o registro na Anvisa. Os lotes nem chegavam a ser testados. Com a mudança, o que já está no mercado poderá continuar sendo vendido até esgotar o prazo de validade ou o prazo do registro, que dura cinco anos.
Assim que houver necessidade de renovar o cadastro, ou a cada novo modelo de prótese lançado, o Inmetro será acionado para testar a resistência do material e a composição do silicone. "Já existiam normas. O que teremos de novo é uma ferramenta de verificação", disse o gerente geral de tecnologia de produtos para saúde da Anvisa, Joselito Pedrosa.
O Inmetro publicou nota esclarecendo que vai atender a solicitação da agência e publicará até o próximo dia 31 os requisitos de avaliação para os implantes mamários. A partir daí importadores e fabricantes poderão se submeter às determinações e começar a vender os novos modelos de silicone.
Apoio
O presidente da Sociedade Brasileira de Cirurgia Plástica, José Horácio Aboudib, afirma que a entidade apoia a mudança. "Somos a favor de todas as medidas que visem a aumentar a segurança dos pacientes", disse. Ao todo, há 50 tipos de próteses mamárias certificadas pela Anvisa e 24 fabricantes credenciados. Três deles são brasileiros e os outros 21 são de fora do país.
A reportagem conversou com empresas nacionais para avaliar o impacto da medida. A Silimed, uma das principais empresas do setor, no mercado há 34 anos, afirmou que "foi pega de surpresa". A Lifesil, que produz implantes de silicone mamários e de glúteos em Curitiba, informou que já é submetida a auditoria da Anvisa e que usa, na composição das próteses, um gel médico produzido nos Estados Unidos e autorizado pela FDA, agência que regula os medicamentos e os alimentos nos EUA.
A nova resolução também estabelece que o cirurgião deverá dizer aos pacientes, com antecedência, quais são os riscos potenciais, as possibilidade de interferência na amamentação, necessidade de avaliação médica periódica e expectativa de uma nova cirurgia quando o produto chegar ao fim da vida útil.
As novas regras foram criadas depois do escândalo internacional envolvendo a marca francesa PIP (Poly Implant Prothèse) e a holandesa Rofil, acusadas de usar silicone inapropriado, com risco de romper ou vazar e provocar problemas de saúde. Calcula-se que 20 mil brasileiras tenham implantes dessas marcas estrangeiras.